近年來多重耐藥細菌的迅速傳播已演變成為全球性的醫療危機,臨床上常見的高毒力、高耐藥性致病菌如屎腸球菌(E. faecium)、金黃色葡萄球菌(S. aureus)、肺炎克雷伯菌(K. pneumoniae)、鮑曼不動桿菌(A. baumannii)、銅綠假單胞菌(P. aeruginosa)和腸桿菌屬(Enterobacter spp.),因其能“逃脫”傳統抗生素的治療而被稱為“ESKAPE”菌。在全球范圍內,ESKAPE菌是醫院感染的主要原因,世界衛生組織將它們定義為需要關鍵/高度優先應對的病原體,這6種病菌中有2種為革蘭氏陽性菌,4種為革蘭氏陰性菌。相比革蘭氏陽性菌,革蘭氏陰性菌由于更復雜的細胞壁結構和高度活躍的外排泵系統,導致其更易產生耐藥性。目前,新抗生素的開發速度遠遠滯后于細菌耐藥性的發展速度,已超過50年無新的抗生素類別被批準用于治療革蘭氏陰性細菌感染。因此,亟需研發具有高選擇抗菌活性且不易引發耐藥的新型抗菌劑,以應對廣泛蔓延的革蘭氏陰性ESKAPE菌感染。
西北工業大學柔性電子研究院黃維院士李鵬教授課題組長期聚焦于應對耐藥菌感染的生物材料與柔性器件研究,近期該課題組合成了一類新型含氟兩親性陽離子聚合物,其能夠選擇性地殺滅多重耐藥的革蘭氏陰性ESKAPE病原體,同時延緩耐藥性的產生。受具有陽離子兩親性結構的天然抗菌肽啟發,該課題組利用可逆加成-斷裂鏈轉移聚合技術(RAFT)合成了一系列含氟兩親性陽離子聚合物,通過可控聚合調控陽離子單體(2-氨基乙基甲基丙烯酸酯鹽酸鹽,AEMA;2-(二甲氨基)乙基甲基丙烯酸酯,DMAEMA)和疏水單體(2,2,3,3,4,4,4-七氟丁基甲基丙烯酸酯,HFBMA)之間的配比,優化分子生物活性(圖1)。相比傳統的疏水烷基,含氟基團具有更優的疏水、疏油以及生物相容性,可提升陽離子聚合物的抗菌活性并降低溶血性。這項研究表明,PAmHFn系列聚合物具有廣譜抗菌性能,而PDmHFn系列聚合物則具有針對革蘭氏陰性菌的選擇殺菌性,可有效殺滅多種革蘭氏陰性ESKAPE耐藥菌株,同時具有良好的哺乳動物細胞相容性和低溶血性,為革蘭氏陰性菌感染的治療藥物研發提供了一種新的研究思路。
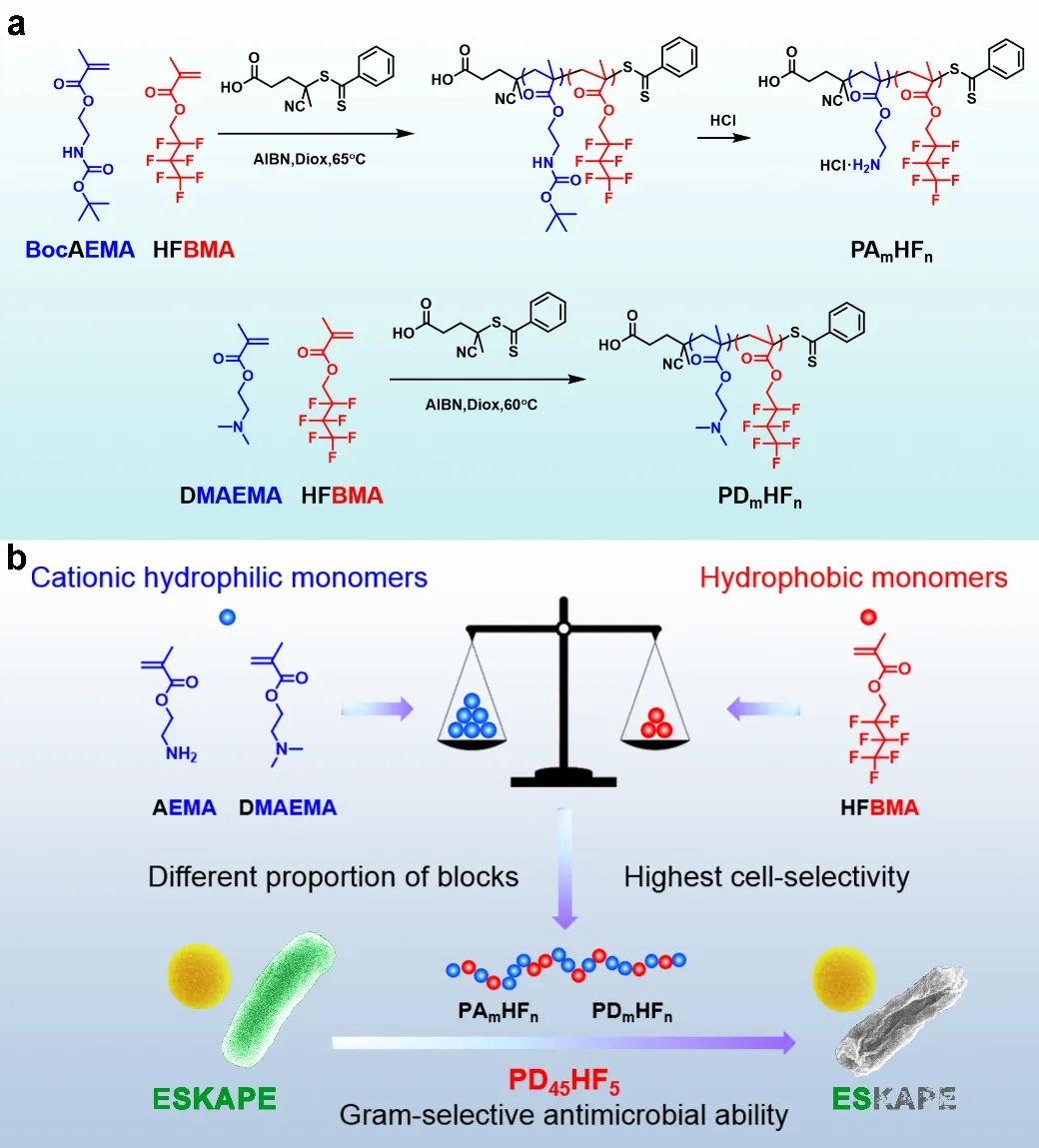
圖1:含氟兩親性陽離子抗菌聚合物的合成和設計,所合成的PAmHFn系列聚合物具有廣譜殺菌性,PDmHFn系列聚合物具有革蘭氏陰性菌選擇殺菌性
研究結果表明,共聚物中含氟鏈段的增加,能夠顯著提升兩親性陽離子抗菌聚合物的抗菌能力。其中,最優的含氟兩親性聚合物(PD45HF5)對于多重耐藥革蘭氏陰性ESAKPE病原體的最小抑菌濃度可低至4-32μg/mL,甚至對于多重耐藥的鮑曼不動桿菌(multidrug resistance A.baumannii,MDRAB)和產超廣譜β-內酰胺酶腸桿菌(extended-spectrumβ-lactam E. coli,ESBL-EC)抗菌性能(最小抑菌濃度可低至4μg/mL)優于一線抗生素左氧氟沙星。最優的PD45HF5聚合物不僅對多重耐藥革蘭氏陰性的ESKAPE病原體具有高效的抗菌活性,同時對哺乳動物細胞表現出較低的細胞毒性(半溶血濃度>4096μg/mL),細胞選擇性(半溶血濃度/最小抑菌濃度)超過1000(圖2)。
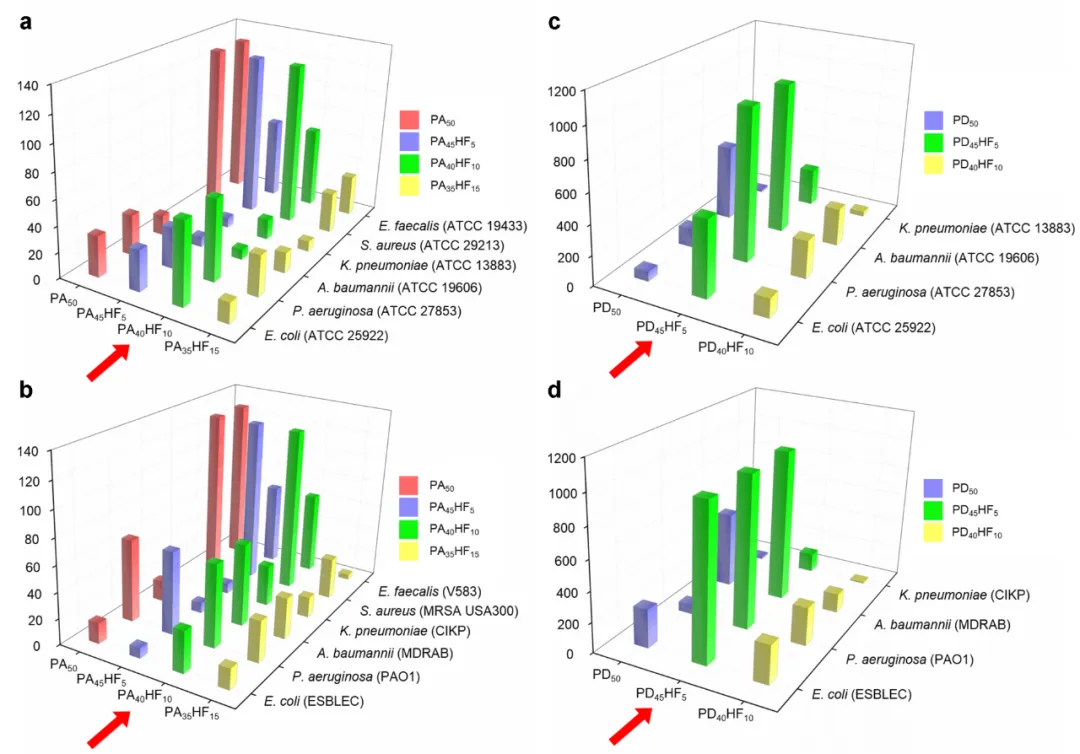
圖2:PAmHFn和PDmHFn的細胞選擇性。a-b: PAmHFn對于實驗室標準和臨床耐藥ESAKPE病原體的細胞選擇性;c-d: PDmHFn對于實驗室標準和臨床耐藥革蘭氏陰性ESAKPE病原體的細胞選擇性。
為了研究兩親性含氟陽離子聚合物的抗菌機理,膜去極化結果表明兩親性含氟聚合物可穿透細菌細胞膜,從而釋放出較強的熒光信號。同時當兩親性含氟聚合物與細菌共孵育后,細胞膜表面出現了不同程度的褶皺、凹陷甚至穿孔,綜上實驗結果證實兩親性含氟聚合物主要以膜破壞的機制發揮抗菌作用(圖3)。
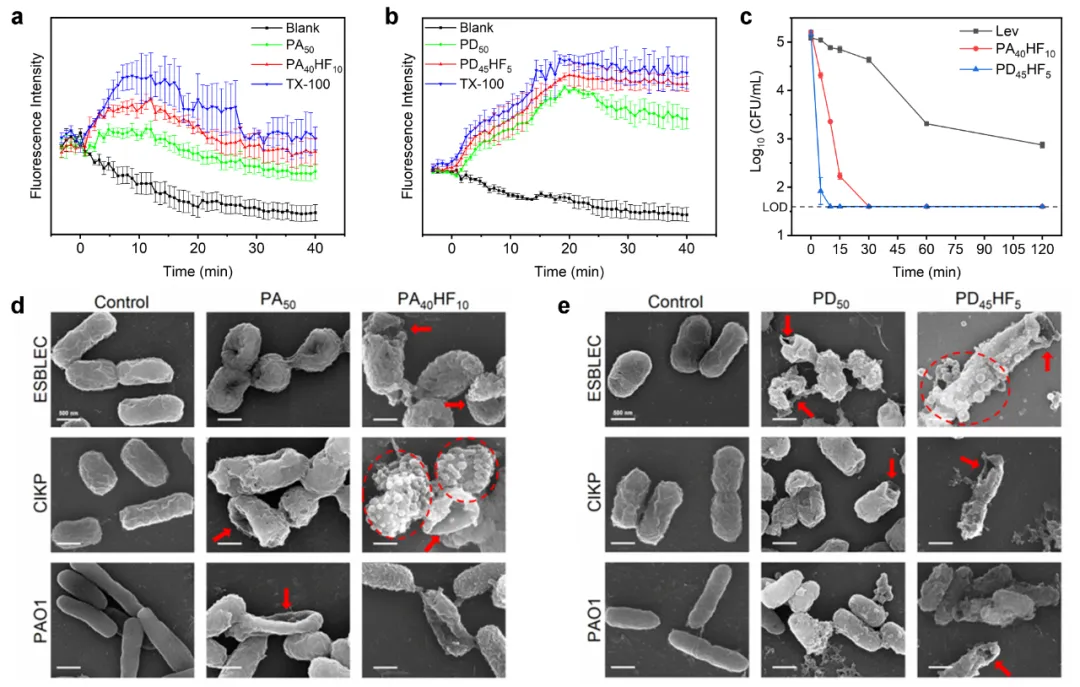
圖3:PAmHFn和PDmHFn的抗菌機理。a-b: PAmHFn和PDmHFn的膜去極化作用;c: PA40HF10、PD45HF5和左氧氟沙星對ESBL-EC的細菌殺傷動力學;d-e:細菌與不同聚合物共孵育后的形貌變化。
此外,兩親性含氟聚合物在延緩耐藥性方面也展現出突出的優點。在連續傳代培養超過100代的條件下,ESBL-EC對傳統抗生素左氧氟沙星產生了明顯的耐藥性,而在同樣條件下未對兩親性含氟聚合物產生耐藥性。為了研究PD45HF5的革蘭氏選擇性抗菌性能,該課題組利用脂多糖抑制試驗進行了探索。與革蘭氏陽性菌不同,脂多糖作為革蘭氏陰性菌外膜的獨特組成部分,結果表明PD45HF5與脂多糖共孵育會以濃度依賴性方式對其抗菌效果造成顯著影響,這可能歸因于PD45HF5與革蘭氏陰性菌表面的脂多糖具有一定的親和作用。因此PD45HF5更易與革蘭氏陰性菌的脂多糖進行結合,從而具有針對革蘭氏陰性菌的選擇殺菌性(圖4)。
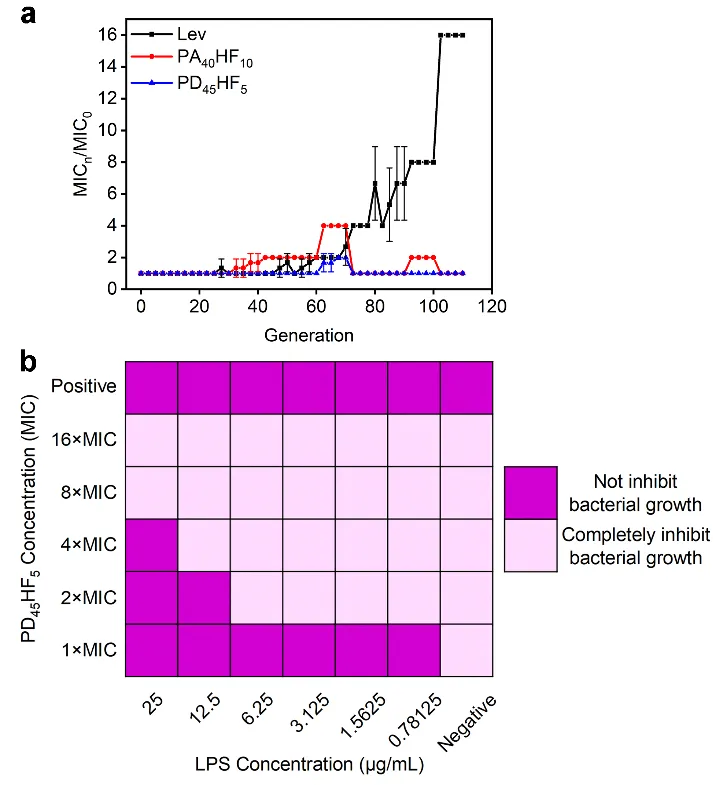
圖4:細菌耐藥性測試和脂多糖抑制實驗結果。
該課題組進一步評估了最優PD45HF5的體內抗感染療效,結果表明在傷口感染和腹膜炎動物模型中均顯示出相當于抗生素的體內治療效果,其顯著降低了感染部位的細菌負荷,展示了其在抗革蘭氏陰性耐藥菌感染方面的治療潛力(圖5)。綜上,含氟兩親性聚合物可作為一種有前景的抗菌劑以特異性針對多重耐藥革蘭氏陰性的ESKAPE細菌感染,在緩解耐藥性方面具有巨大潛力。
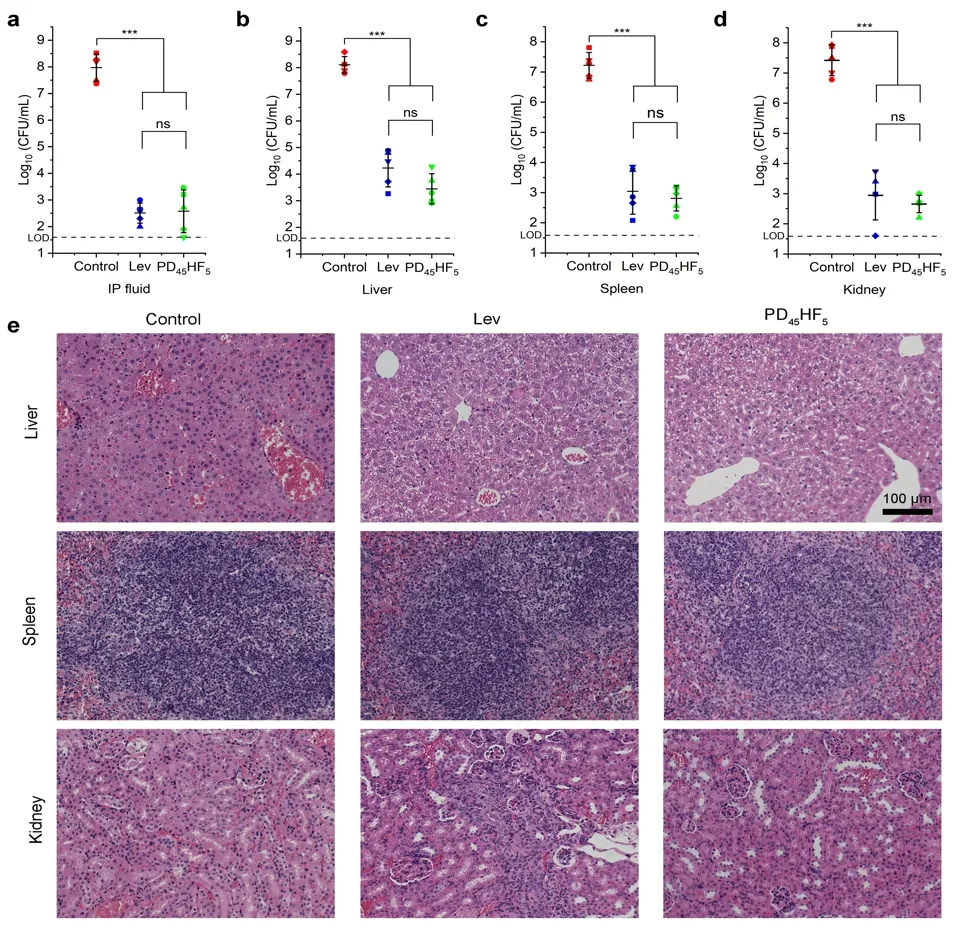
圖5:體內腹膜炎感染模型。a-d:腹腔積液、肝、脾、腎中細菌計數;e:不同材料處理后腹部器官的蘇木精-伊紅染色染色圖像。
相關工作以Fluoroamphiphilic polymers exterminate multidrug-resistant Gram-negative ESKAPE pathogens while attenuating drug resistance為題發表在Science Advances上。西北工業大學柔性電子研究院李鵬教授為本文通訊作者,2023屆博士生畢業生周倩和2022屆碩士畢業生李琨鵬為共同第一作者。該工作得到了國家自然科學基金,陜西省自然科學基礎研究計劃等項目的支持。
論文信息:
Qian Zhou?, Kunpeng Li?, Kun Wang, Weilin Hong, Jingjie Chen, Jin Chai, Luofeng Yu, Zhangyong Si, Peng Li*. Fluoroamphiphilic polymers exterminate multidrug-resistant Gram-negative ESKAPE pathogens while attenuating drug resistance. Science Advances, 2024, 10(35), eadp6604.
文章鏈接:https://www.science.org/doi/10.1126/sciadv.adp6604
(文字:周倩、劉亞妮;審核:王學文)